La cristallografia nella didattica chimica
Quando insegnavo al biennio dell’I.T.I.S. di Arezzo chimica di base una delle prime lezioni del corso era dedicata alla illustrazione di una esperienza di laboratorio che gli studenti avrebbero eseguito a casa. Si trattava della formazione di cristalli di cloruro di sodio da una soluzione del sale. Dopo circa una settimana ciascun studente portava a scuola il suo piattino dove erano cresciuti piccoli ma regolari cristalli cubici di salgemma.
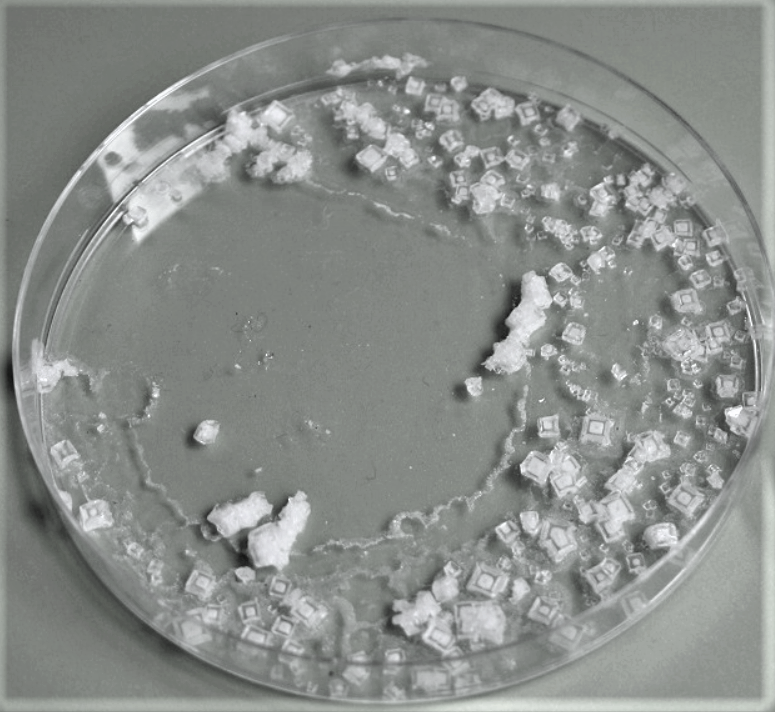
 Formazione di cristallli di cloruro di sodio Cristalli di cloruro di sodio al microscopio
Formazione di cristallli di cloruro di sodio Cristalli di cloruro di sodio al microscopio
Dopo aver esaminato ciascuno la propria collezione di cristalli, si passava nell’aula di microscopia per osservare i cristalli ingranditi. La visione dell’abito dei cristalli era una esperienza che entusiasmava molto i ragazzi.
La cristallizzazione
A questa esperienza ne seguiva un’altra, più avanti nel corso, questa volta nel laboratorio della scuola. La classe era divisa a gruppi di due studenti ciascuno. Ciascun gruppo aveva a disposizione due provette, un becher per il bagnomaria e due soluti, il cloruro di ammonio e il nitrato di potassio. Dopo aver preparato nella provetta a caldo una soluzione di un soluto, la provetta veniva tolta dal bagnomaria e fatta raffreddare lentamente a temperatura ambiente. Quando la soluzione raggiungeva il punto di saturazione aveva inizio la formazione di bellissimi cristalli che avevano la forma dei fiocchi di neve nel caso del cloruro di ammonio e di lance allungate del nitrato di potassio.
Formazione di Cristalli di Nitrato di Potassio a forma di lance


La cristallizzazione del cloruro di ammonio


Formazione dei cristalli in provetta come ficchi di neve Crescita dei cristalli del cloruro di ammonio al miscoscopio
L’esperienza forniva l’occasione di parlare di solubilità e di soluzioni sature. Una variante dell’esperienza era di fare cadere una goccia delle soluzioni in un vetrino e osservare la formazione e la crescita dei cristalli. Quest’ ultima parte dell’esperienza era adatta soprattutto dopo aver fatto l’esperienza del salgemma, all’inizio del corso.
Perchè i cristalli
Osservare i cristalli, la loro formazione e la loro crescita è stato uno dei fenomeni che più ha contribuito nella storia della scienza a far maturare il concetto di struttura discontinua e particellare della materia. Riproporre agli studenti il fenomeno della formazione dei cristalli, discutendone le possibili spiegazioni è un modo concreto di dare una risposta all’ipotesi, che è di per sé molto astratta, della struttura discontinua della materia. E tutto questo prima di parlate di atomi che non rappresentano una “risposta” appagante della struttura discontinua della materia per il nostro studente al primo anno di s.s.s., ma è semplicemente una nozione in più da imparare.
I contributi della cristallografia
Nella storia della scienza e in particolare della chimica ha avuto un ruolo fondamentale lo studio dei cristalli sotto diversi aspetti. Abbiamo già detto come l’ipotesi corpuscolare della materia abbia trovato riscontro nelle proprietà dei cristalli, ma il loro studio ha condotto anche alla scoperta dell’isomeria ottica dei cristalli e delle molecole costituenti i cristalli. Quest’ultima ha permesso che fosse concepito il carbonio tetraedrico nelle molecole organiche. Questa affascinante storia ci viene raccontata da due giovani chimici Kresimir Molcanov e Vladimir Stilinovic´dell’Università di Zagabria . Ho tradotto il loro saggio che trovate in allegato in PDF. Ce la propongono ripercorrendo le tappe essenziali dello sviluppo della cristallografia chimica prima dell’impiego della diffrazione a raggi X in modo sintetico e accattivante.
Il saggio di storia della cristallografia chimica




